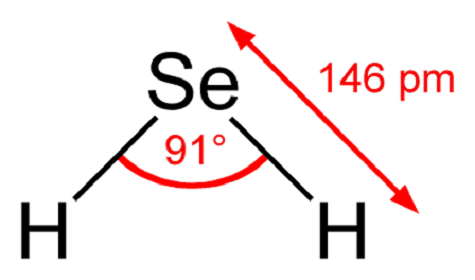
Conocido como seleniuro de hidrógeno o hidruro hiposelenioso, el ácido selenhídrico es un hidrácido muy empleado por la industria química para obtener otros compuestos inorgánicos.
Cómo se obtiene el ácido selenhídrico.

El ácido selenhídrico se origina de la unión de dos moléculas de hidrógeno con un átomo calcógeno, como es el selenio, que además es un elemento que forma parte del grupo 16 de la tabla periódica, como igualmente lo son el oxígeno, el azufre o el teluro, entre otros.
Hay que tomar en cuenta, que el selenio simple se obtiene por medio de la síntesis de la selenita con ácido ascórbico o hidracina hidrocloruro, e industrialmente, el ácido selenhídrico se consigue sometiendo al selenio a elevadas temperaturas con hidrógeno en forma gaseosa.
Propiedades que caracterizan al ácido selenhídrico.
Normalmente, el ácido selenhídrico es un gas incoloro inflamable que presenta un olor característico a huevo podrido. Siendo el derivado más tóxico del selenio, en contacto con elementos oxidantes, agua e hidrocarburos halogenados, se descompone formando gases venenosos e inflamables como el dióxido de selenio, que a veces puede ser liberado en forma de fuego.

Asimismo, éste hidrácido tiene la capacidad de precipitar muchos elementos metálicos, constituyendo un agente reductor más potente que el sulfuro de hidrógeno. Indistintamente en soluciones acuosas, el seleniuro de hidrógeno se oxida con gran facilidad debido a su sensibilidad al oxígeno, originando un precipitado de color rojizo, en este sentido, se puede decir que siendo más fuerte que el ácido sulfhídrico, ambos elementos poseen las mismas propiedades de solubilidad en agua.
Es importante señalar que la exposición a este compuesto puede causar daños pulmonares agudos, lesiones oculares e incluso hasta la muerte.
Qué aplicaciones tiene el ácido selenhídrico.

A pesar de su toxicidad, el ácido selenhídrico es un gas industrial muy importante, ya que sirve para preparar seleniuros metálicos y compuestos seleniados a partir de nitrilos y alquenos, usados por la industria metalúrgica en la preparación de materiales semiconductores, o por los laboratorios como reactivo químico para la síntesis de algunos componentes.
Al ser potencialmente explosivo en contacto con el aire o incluso con alguna chispa, el ácido selenhídrico se almacena en cilindros de acero reforzados con carbono y cerrados bajo presión, de esta manera, se minimiza la posibilidad de alguna fuga y se alarga su vida útil hasta un máximo de 18 meses, haciéndolo un concentrado con casi un cien por ciento de pureza y muy apto para el uso industrial.