¿Qué es un ácido?
La palabra ácido deriva del término latín acidus que significa agrio o amargo. Los ácidos son una sustancia que al entrar en contacto con el agua incrementa la concentración de iones de hidrógeno, y al combinarse con bases se forman sales.
Una base es aquel elemento que posee alcalinidad que en combinación con un ácido produce sal y agua, reacción que se denomina ácido base. Dependiendo de la temperatura los ácidos pueden ser sólidos, líquidos o gaseosos, y por su forma se presenta como sustancia pura o solución.
Normalmente consumimos muchos alimentos como el limón, entre otros, que tienen un sabor ácido, a pesar de esta sensación, el limón al entrar en nuestro organismo es el alimento más alcalino que existe.
En las diferentes teorías del ácido base, se define al ácido de la siguiente manera:
- Ácido de Arrhenius (1884).
El químico sueco Svante Arrhenius, lo define como un elemento químico capaz de liberar iones de hidrógeno en un líquido.
- Ácido Brönsted-Lowry (1923).
Para los químicos Johannes Brönsted y Thomas Lowry es una sustancia capaz de emitir un protón.
- Ácido Lewis (1923).
Gilbert Lewis, fisicoquímico norteamericano, lo conceptualiza como una especie que acepta par de electrones de otro elemento, para lograr estabilidad.
Propiedades del ácido
Los ácidos se distinguen por poseer las siguientes particularidades:
Poseen un sabor desagradable y amargo.
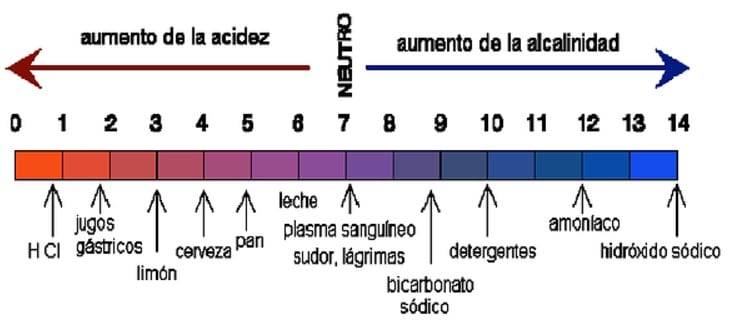
Cambian de tonalidad con los indicadores de pH, por ejemplo el papel tornasol azul se transforma en rosado, y el de metilo de naranja toma un color rojo, siendo su nivel de pH superior a 7.
Es un elemento altamente abrasivo.
Desprende hidrógeno al mezclarse con algunos metales activos.
Posee una apariencia viscosa.
Logra ocasionar quemaduras en la piel.
Crea efervescencia cuando entra en contacto con el mármol.
Si está concentrado destruye los tejidos biológicos.
Excelente conductor de electricidad en medios acuosos.
Reacciona con las bases y óxidos metálicos formando sal y agua.
Tiene efecto al mezclarse con carbonatos, bicarbonatos y sulfuros metálicos.
Sus propiedades desaparecen al momento de interactuar con las bases.
Clasificación del ácido

Se puede categorizar el ácido en dos grandes grupos de acuerdo a su composición:
- Inorgánico o mineral, está compuesto por hidrógeno y otros elementos excepto carbono, que en una mezcla acuosa produce iones de hidrógeno.
Sus características son que neutraliza las bases, sin agua es gaseoso o sólido, y se divide en oxácidos y en hidrácidos.
- Orgánico, su estructura se basa en la sustitución de algunos átomos de hidrógeno, por uno de oxígeno y un grupo hidroxilo.
No se disuelven en agua sino en soluciones orgánicas y son menos reactivos que los ácidos inorgánicos.
Reaccionan con las bases produciendo sales y con alcoholes esteres.
Pueden ser monocarbolíxicos, dicarbolíxicos, policarbolíxicos y sulfónicos.
Están clasificados de la siguiente manera:
-
Por el número de iones de hidrógeno:
Monopróticos: poseen en su estructura molecular un hidrógeno (ácido nítrico)
Dipróticos: la complexión está formada por dos átomos de hidrógeno (ácido carbónico).
Polipróticos: constituido por tres moléculas de hidrógenos (ácido fosfórico).
-
En base a la capacidad de ionización:
Débiles: su nivel de ionización en agua es bajo o parcial, dando lugar a una reacción de equilibrio (ácido etanoico).
Fuertes: posee un proceso de ionización completa en agua, donde se llegan a donar todos sus protones (ácido nítrico).
Tipos de ácidos
Los ácidos más comunes y sus aplicaciones

Usualmente el ácido se emplea en los procesos industriales o químicos, y de acuerdo a su clasificación encontramos los siguientes usos:
Ácidos minerales o inorgánicos:
Clorhídrico: se usa en el refinamiento de minerales de estaño, para convertir el almidón de maíz en jarabe y como curtidor en la industria del cuero.
Sulfúrico: se utiliza en el papel encerado, refinación de aceites vegetales, extracción de uranio, y desoxidación de hierro y acero.
Perclórico: en la industria de explosivos, como disolvente de metales y aleaciones.
Sulfámico: usado en el tratamiento de superficies, como blanqueador en la elaboración del papel, y estabilizante del cloro en las piscinas.
Nítrico: en la fabricación de fertilizantes, explosivos y en la metalurgia.
Ácidos sulfónicos:
Generalmente se prestan para productos de limpieza para pisos, superficies duras y baldosas de baño.
Bencensulfónico: es aplicado en la deshidratación y una gran variedad de fármacos.
Metansulfónico: aparece en los limpiadores aerosoles multi-uso.
Ácidos carboxílicos:
Sórbico: es usado en la elaboración de conservantes, plásticos y lubricantes.
Acético: está presente en el vinagre, disolvente de pinturas, películas fotográficas y cauchos.
Cítrico: es un ingrediente para las bebidas carbonatadas.
Propiónico: sirve como ayudante en la maduración del queso suizo.
Acetilsalicílico: es la base para formular analgésicos, antipiréticos y antiinflamatorios.
Acrílico: se emplea en la creación de barnices, resinas elásticas y adhesivos transparentes.
Oleíco: en la fabricación de detergentes, champú y otros cosméticos.
Ácidos carboxílico vinílogos:
Ascórbico: es el componente esencial para la vitamina C.
El ácido en los alimentos

Cómo se mencionaba en un principio, el sabor ácido de los alimentos no tiene nada que ver con su efecto en el organismo, debido a la cantidad de reacciones químicas que cambian sus propiedades nutritivas.
Más bien, el que un alimento contenga ácido está determinado por su contenido de minerales y principalmente cómo reacciona con el pH cuando entra en el organismo.
Mientras el alimento baje el pH al interactuar en el cuerpo será más ácido, deteniendo el crecimiento de bacterias.
Uno de los principales minerales que usa el cuerpo para neutralizar la acidez en la sangre es el calcio que proviene de los huesos y dientes.
Entre los alimentos con mayores propiedades acidificantes se encuentran el café, todos los productos procesados, azúcar, harina refinada, leche y productos lácteos, maíz, lentejas, calabaza, productos de pastelería y panaderías, arroz, pasta, galletas, bebidas artificiales y alcohol.
También los ácidos grasos saturados como el palmítico y esteárico vienen en las grasas animales y el chocolate.
Los ácidos grasos insaturados como el oleico, linóleico y araquidónico se presentan en los aceites de origen vegetal, pescados y mariscos, conocidos por su alto contenido de Omega 3.
El ácido butírico está incluido en la mantequilla, queso parmesano, y leche cruda, mientras que el ácido caprílico se encuentra en la leche materna y el coco.

