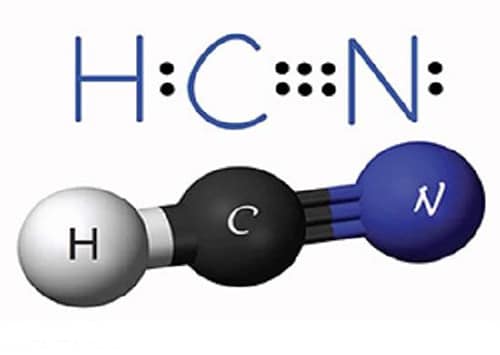
Actualmente el ácido cianhídrico es un componente muy usado en la industria química, sin embargo, detrás de este compuesto se esconde un oscuro pasado. Siendo un elemento producido en grandes cantidades en el mundo entero, fue aislado por primera vez a partir del tinte azul de Prusia, y es conocido también por los nombres de cianuro de hidrógeno, ácido prúsico, metanonitrilo o formonitrilo.
Este químico de acción rápida y potencialmente mortal, que impide que las células del cuerpo utilicen el oxígeno en forma apropiada, fue usado durante la II Guerra Mundial en los campos de concentración nazi como método de exterminio a millones de judíos, debido a su bajo costo de producción, y hoy en día se utiliza en las ejecuciones con cámara de gas en los Estados Unidos.
Cómo se obtiene el ácido cianhídrico.

La forma más elemental de obtener ácido cianhídrico es mezclando cianuro con agua, aunque también, se puede producir por la simple combustión de la madera, la cual genera altas concentraciones de monóxido de carbono. Igualmente, las frutas con semillas grandes, como el albaricoque o las almendras, contienen pequeñas cantidades de cianuro en sus simientes. Además, se encuentra en los gases emitidos por los vehículos, en el humo del tabaco o en la combustión de algunos plásticos.
Ahora bien, existen algunos procesos químicos para producir éste peligroso componente, como:
Oxidación Andrussov.
Un mecanismo inventado por el ingeniero químico alemán Leonid Andrussow, en 1927, en la cual el metano y el amoníaco reaccionan ante el oxígeno, sometidos a altas temperaturas mediante un catalizador de platino, creándose la oxidación necesaria para la obtención de ácido cianhídrico.
Proceso BMA o Degussa.

Superando algunos inconvenientes del mecanismo de Andrussov, se emplea un hidrocarburo alifático, es decir, de carbono o hidrógeno, mezclado con amoníaco y un impulsor de platino, sin usar oxígeno, lográndose el ácido indirectamente a través de la pared del reactor, por el vapor originado en la reacción.
Shawinigan.
A pesar de ser relativamente refinado y con costos elevados, es un procedimiento caldeado mediante energía eléctrica, donde el amoníaco y el gas natural son calentados con electrodos de alta tensión, produciéndose el ácido.

También en los laboratorios, se produce ácido cianhídrico, añadiendo ácidos sobre sales de cianuro de metales alcalinos, que habitualmente puede originar envenenamientos accidentales, ya que estos ésteres se convierten en cianuro gaseoso.
Cuáles son las propiedades del ácido cianhídrico.

El ácido cianhídrico posee un color ligeramente azul con un olor almendrado, siendo muy soluble en agua, venenoso, altamente volátil e incompatible con materiales combustibles, bases, aminas, oxidantes y otros ácidos.
Usualmente, el aliento de la persona intoxicada desprende un hedor a almendra, ya que este ácido tras llegar a la sangre por vía respiratoria, provoca la inhibición de las enzimas que transportan el oxígeno a las células, produciéndose la pérdida de la consciencia, rigidez corporal y asfixia mecánica, que en dos o tres minutos genera la muerte del intoxicado.
Qué usos tiene el ácido cianhídrico.

Principalmente el ácido cianhídrico es aplicado por la industria química en numerosos procesos de producción, como en la fabricación de tintes o sustancias explosivas. Aparte, es el generador del cianuro de sodio y el cianuro de potasio, empleado en las actividades mineras. Asimismo, por medio de las cianohidrinas se preparan una gran cantidad de compuestos como el monómero metacrilato de metilo, de la acetona y el aminoácido de metionina, y agentes quelantes como el ácido etilendiamino tetraacético (EDTA) o el ácido nitriolotriacético (NTA). Mediante el mecanismo de hidrocianación se logra el compuesto orgánico primordial para la elaboración del nylon 6.6.
En fin, el ácido cianhídrico a pesar de ser débil, constituye un componente químico altamente peligroso para el ser humano.