Conocido por sus nombres ancestrales como aguafuerte o espíritu de nitro, el ácido nítrico es en la actualidad uno de los más usados a nivel industrial.
Siendo el oxácido más importante derivado del nitrógeno, el ácido nítrico es un compuesto químico inorgánico altamente tóxico.
También llamado ácido azótico o hidróxido de nitrilo, se obtiene de la mezcla del óxido de nitrógeno con agua.
Descubierto en 1648, por el alquimista Jabir ibn Hayyan, cuando quemaba una mezcla de nitro, alumbre y sulfato de cobre.
Posteriormente, el químico alemán Glauber mejoró su obtención destilando nitrato de potasio con ácido sulfúrico.
En 1784, Henry Cavendish determinó que podía ser sintetizado pasando una chispa de corriente eléctrica a través del aire húmedo.
Al respecto, el ácido nítrico está presente en la atmósfera y en la lluvia en forma de pequeñas partículas.
A raíz del procedimiento desarrollado por el químico alemán Wilhelm Ostwald en 1902, el ácido nítrico, se empezó a obtener industrialmente a partir de la síntesis del amoníaco con el oxígeno presente en el aire, mediante catalizadores de platino.
Propiedades del ácido nítrico.

Las principales características del ácido nítrico
- Su consistencia es líquida, aceitosa e incolora, aunque a veces toma una coloración amarilla debido a su descomposición por la acción de la luz, por esta razón su almacenamiento se realiza en frascos de vidrio ahumado.
- Altamente soluble en agua formando un azeótropo que permite su calentamiento.
- A temperatura ambiente libera humos blancos o amarillos, y en altas concentraciones posee un fuerte olor irritante.
- Se descompone por calentamiento creando agua, oxígeno y dióxido de nitrógeno.
- Es un ácido muy corrosivo que ataca a la mayoría de los metales, excepto el platino y el oro.
- Al contacto con polvos metálicos, carburos y sulfuro de hidrógeno, genera reacciones explosivas.
- En metales como el aluminio y cromo produce una capa de óxido que impide la corrosión de otros elementos químicos.
- Origina sales en la reacción con óxidos o sustancias básicas, y aunque no es inflamable, facilita la combustión tanto en la madera como en la gasolina.
- Concentrado tiene un efecto nitrificante sobre materiales orgánicos, en cambio diluido los oxida.
- Reacciona de forma violenta con sustancias como la acetona, ácido acético, alcoholes y trementina, causando riesgo de fuego o formación de gases tóxicos.
Aplicaciones del ácido nítrico.

El ácido nítrico es utilizado en el área industrial, pero de la misma manera, en los sectores de química y salud, se incluye en diferentes procesos:
- En la producción de abono nitrogenado, por parte de la industria de fertilizantes.
- Como nitrocompuesto en la elaboración de colorantes artificiales para la industria fotográfica.
- Aprovechado para la fabricación de explosivos como el TNT, dinamita y algodón pólvora o nitrocelulosa.
- Es un componente químico empleado por la industria de productos de limpieza, para tuberías y sumideros.
- El sector joyero lo aplica en el grabado de metales y en la comprobación del oro y el platino.
- Forma parte del procedimiento de obtención de ácido adípico para la confección de fibras sintéticas especiales, nylon y autopartes plásticas.
- Se elaboran poliuretanos que sirven para producir espumas, pinturas y selladores de superficies.
- Junto con otros ácidos se emplea en la fase de neutralización durante el tratamiento de aguas residuales.
- Ampliamente usado en la preparación de la nitroglicerina, como medicamento para tratar enfermedades del hígado, anginas de pecho, infarto al miocardio e insuficiencias coronarias, debido a su poderosa acción vasodilatadora.
- Constituye un ingrediente en la elaboración de tópicos dermatológicos para el tratamiento de verrugas o papilomas.
- La medicina veterinaria ha aprovechado sus propiedades diuréticas y antisépticas en la cura de padecimientos de animales.
Normalmente, la venta comercial del ácido nítrico suele realizarse en bajas concentraciones de hasta un 68%, sin embargo, su condensación más alta se conoce como ácido nítrico fumante.
Efectos en la salud del ácido nítrico.
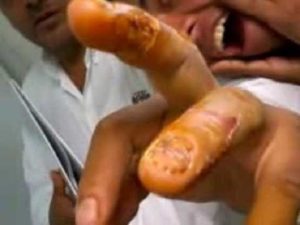
A pesar de los diferentes beneficios que tiene el ácido nítrico, en su estado líquido o en vapor, representa un componente peligroso que puede causar efectos nocivos para la salud:
- Siendo una sustancia corrosiva es irritante para los ojos provoca lagrimeo, erosión de la córnea e incluso ceguera.
- Causa graves ulceraciones y quemaduras en membranas o tejidos como la boca, garganta, esófago, estómago y erosión dental.
- En forma retardada puede originar daños en el tracto respiratorio, así como también edemas pulmonares, bronquitis y neumonía.
- Conduce al desarrollo de un pulso rápido y débil, dilatando el corazón e incluso originando la muerte por colapso circulatorio.
- Los vapores del ácido nítrico contienen trazas de metales que se han relacionado con el cáncer en la laringe.
- Al contacto con la piel, puede propiciar un color amarillento en la epidermis, dermatitis y quemaduras severas.
Por ello es de suma importancia, que toda persona que entre en contacto con este compuesto debe tomar las medidas preventivas y procedimientos establecidos en las normas de seguridad industrial, y así evitar que un incidente se transforme en tragedia.